Диффузная субэндокардиальная ишемия на ЭКГ. Ствол? 3-сосудистая болезнь? Нет!
Случай прислан из Wake Forest, авторы: Джейсон Стопайра, Шеннон Мумма, Шон О'Рурк и Брайан Хистэнд.
Отредактировал Смит (Diffuse Subendocardial Ischemia on the ECG. Left main? 3-vessel disease? No!). Продолжение дискуссии, начатой 17 декабря 2020 (Крайне выраженная диффузная депрессия ST с элевацией ST в aVR. Что вы думаете?)
СЛУЧАЙ
52-летний мужчина с анамнезом гипертонии и ХОБЛ вызвал скорую помощь из-за боли в груди, слабости и тошноты. Первоначальное впечатление фельдшера о пациенте заключалось в том, что пациент выглядел серьезно больным. У пациента были отмечены психические нарушения, кожа была пепельной. Первоначальное артериальное давление составляло 80 (пальпаторно) с частотой сердечных сокращений 104, ЧДД 20, сатурацией кислорода 94%, а глюкоза крови составила 14 ммоль/л. В остальном - при аускультации были слышны хрипы, отмечено увеличение времени заполнения капилляров, замедление и трудности при выполнении команд и ответов на вопросы.
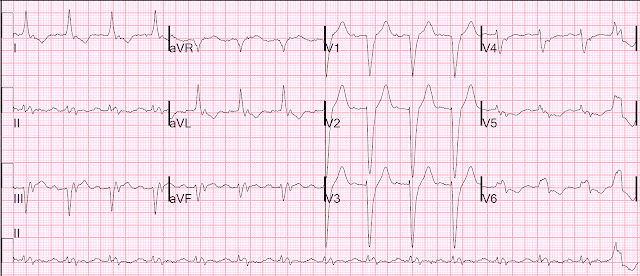
Немедленно была записана ЭКГ в 12 отведениях:
Элевация ST в отведениях aVR и V1 с выраженной депрессией ST в I, II, III, aVF, V3-V6.
Что необходимо сделать?
Следует ли назначать экстренную катетеризацию?
Комментарий Смита:
Этому пациенту не проводилось прикроватное ультразвуковое исследование. Если бы оно было выполнено, то выявило бы особенность, которая очевидна на этом УЗИ (однако функция ЛЖ у нашего пациента в тот момент не была бы такой хорошей, как на этой записи):
Запись сделана над ЛЖ справа.
Посмотрите на выходные пути аорты. Что Вы видите? Ответ ниже на рисунке.
ДАЛЬНЕЙШЕЕ РАЗВИТИЕ КЛИНИЧЕСКОЙ СИТУАЦИИ
Фельдшер связался с ближайшей клиникой, передав «Код ИМпST» и доставил пациента почти за 50 миль в ближайший медицинский центр с возможностями проведения ангиографии. По дороге был дан аспирин 325 мг перорально, но нитроглицерин не давался из-за начальной гипотензии. Кроме того, пациенту была введена жидкость до 750 мл с временным улучшением артериального давления.
Пациент был доставлен прямо в рентгеноперационную для ЧКВ, минуя приемный покой. В рентгеноперационной АД пациента оставалось низким. Диагностическая коронарная ангиограмма выявила только минимальные изменения коронарной артерии, но выявила значительно кальцинированный, «неподвижный» аортальный клапан. На ангиограмме аорты расслоения не выявлено. Во время процедуры у пациента увеличилась потребность в кислороде, и его интубировали для защиты дыхательных путей и оксигенации. Трансторакальная эхокардиограмма показала ФВ ЛЖ менее 15%, критически тяжелый стеноз аорты, тяжелую ГЛЖ и небольшую полость ЛЖ. Пациент был доставлен в палату реанимационного отделения для дальнейшего лечения, где ему в легочную артерию был установлен катетер.
Вот изображение с УЗИ выше:
На этом кадре показана интересующая вас область:
- На аортальном клапане имеется гиперэхогенная зона.
- Это склероз аорты, который в значительной степени связан со стенозом аорты.
- Если вы это видите, вам следует выполнить допплерографию клапана.
- Аортальный клапан в этом примере также имел критический стеноз по допплерографии.
Пациент продолжал оставаться гемодинамически нестабильным, с низким сердечным выбросом и очень высоким давлением наполнения ЛЖ. Несмотря на использование нескольких вазопрессоров в высоких дозах, сохранялась гипотензия. На следующий день пациенту была выполнена баллонная вальвулопластика аорты по поводу тяжелого симптоматического стеноза аорты с гипотензией и симптомами IV класса по NYHA. После вальвулопластики градиент давления у пациента улучшился, но все еще был значительным. Пациенту продолжалась терапия вазопрессорами в больших дозах, но гипотензия сохранялась. Примерно через семь часов после вальвулопластики, у него была асистолическая остановка сердца.
ОБСУЖДЕНИЕ
ЭКГ записанная «по скорой» у этого пациента показала тяжелую ишемию с глубокой «нижнебоковой» депрессией ST и реципрокной элевацией ST в отведении aVR. Хотя это считается «эквивалентом ИМпST», и рекомендации ACC/AHA 2014 г даже одобряют тромболитики для ОКС с такой ЭКГ, обычные критерии, используемые для назначения экстренной катетеризации при ИМпST, не соответствуют этой ЭКГ.
Комментарий Смита:
Помните, что депрессия ST не локализуется в области ишемии, поэтому, термин «нижне-боковая» не говорит вам, где находится ишемия - фактически, это диффузная субэндокардиальная ишемия. Элевация ST в отведении aVR обратна этой депрессии ST при диффузной субэндокардиальной ишемии; вектор депрессии ST направлен к II и V5 и, следовательно, вектор подъема ST направлен к aVR.
Автор продолжил:
Элевация ST в aVR часто возникает из-за обструкции левой коронарной артерии (OR 4,72) и связана с внутрибольничной смертностью от сердечно-сосудистых заболеваний (OR 5,58).1 Элевация ST на 1 миллиметр или более оказалась чувствительной на 80% и 90% специфичной для тяжелой болезни левой коронарной артерии и/или трех сосудов, при которой, в ряде случаев, может потребоваться аортокоронарное шунтирование.2 Знающий фельдшер распознал такую вероятность и сообщил о вероятном ИМпST.
Комментарий Смита:
Я бы изменил приведенное выше утверждение на: «При ОКС, элевация ST в aVR часто возникает из-за обструкции ствола левой коронарной артерии или трех сосудов...» ЭКГ не может диагностировать этиологию ишемии; а только наличие ишемии любой этиологии. Диффузная субэндокардиальная ишемия чаще возникает из-за несоответствия спроса и предложения при отсутствии ОКС, чем из-за ОКС. Распространенными причинами несоответствия спроса и предложения являются гипоксия, тахиаритмии, гипотензия (по любой причине), анемия, стеноза коронарной артерии без ОКС или (внутрижелудочковой) гипертензии.
Доставка кислорода определяется:
1) кислородной емкостью крови,
2) насыщением O2 и
3) коронарным потоком.
Таким образом, при отсутствии атеротромботического механизма (ОКС) ишемия миокарда может быть вызвана:
- Гипотонией (диастолическая гипотензия, поскольку весь коронарный кровоток происходит во время диастолы, потому что внутримиокардиальное давление во время систолы останавливает кровоток). Гипотония, конечно, может быть результатом бради- или тахиаритмии.
- Гипоксией, включая яды окислительного фосфорилирования, такие как HS, CO, CN.
- Анемией или отравлением гемоглобина, такие как метгемоглобин или СО.
- Фиксированным коронарным стенозом, ограничивающий кровоток.
Потребность в кислороде определяется:
1) Постнагрузкой (высокое сопротивление оттоку ЛЖ), которое увеличивается из-за повышенного артериального давления или стеноза аорты.
2) ЧСС: синусовая тахикардия
- У этого пациента уменьшилась доставка (гипотензия) и увеличилась потребность из-за 1) высокой постнагрузке (давление в ЛЖ очень высокое из-за сопротивления оттоку вследствие стеноза аорты) и 2) высокой частоты сердечных сокращений.
- Случай демонстрирует, что аускультация сердца может нести определенную ценность для выявления шума в аорте. Фактически, прикроватное ультразвуковое исследование может даже обнаружить серьезный стеноз аорты. Если вы умеете пользоваться Допплером, вы можете его диагностировать.
Комментарий авторов: Кардиогенный шок на фоне тяжелого стеноза аорты.
Пообщавшись с фельдшером и бригадой интервенционистов, я был готов увидеть тяжелую ишемическую болезнь сердца (ИБС), но сосуды не были стенозированы. Тяжелый стеноз аорты (АС) у этого пациента и связанный с ним тяжелый кардиогенный шок, вероятно, привели к такой ЭКГ-картине, обернувшейся очень сложной проблемой для нашей стационарной бригады.
По сути, кардиогенный шок (КШ) - это проблема снижения сердечного выброса. КШ может быть вторичным по отношению к множеству факторов, включая снижение сократимости сердца (например, инфаркт миокарда), аритмию, патологию клапанов, шунты или обструкцию оттока.
Как и в других случаях шока, может быть рассмотрена первоначальная интенсивная терапия жидкостью. При кардиогенном шоке жидкость может усугубить отек легких, связанный с острой сердечной недостаточностью, но все же может потребоваться для поддержания гемодинамического статуса пациента.
Руководства Американской кардиологической ассоциации не менялись в течение десятилетий с рекомендациями в отношении положительных инотропных агентов, таких как добутамин и дофамин, в случаях кардиогенного шока.3 Имеются данные, свидетельствующие о том, что использование субмаксимальных доз добутамина и дофамина в сочетании, скорее, чем использование одного препарата, приносит пользу пациенту. Преимущества включают улучшение среднего АД и сердечного выброса пациента при минимизации количества кислорода в миокарде, используемого с повышенным сердечным выбросом (СВ).4 Это очень важно, поскольку у этих пациентов уже могла быть какая-либо ишемия сердца. Это было особенно важно для представленного выше пациента, учитывая исходное увеличение потребления кислорода, наблюдаемое при АС из-за обструкции оттока.
Комментарий Смита:
В большом рандомизированном исследовании дофамина и норэпинефрина (11) для лечения шока, которое было опубликовано после вышеупомянутых рекомендаций, дофамин имел больше побочных эффектов (особенно тяжелых нарушений ритма и особенно фибрилляции предсердий). В подгруппе пациентов с кардиогенным шоком дофамин имел статистически значимое повышение смертности на 33% по сравнению с норэпинефрином. Таким образом, норэпинефрин - лучший выбор при кардиогенном шоке (как у этого пациента), чем дофамин или добутамин. Добутамин может быть предпочтительным у пациентов без тяжелой гипотензии с высоким сосудистым сопротивлением.
- De Backer D et al. Comparison of Dopamine and Norepinephrine in the Treatment of Shock. NEJM 362(9):779; March 4, 2009.
Автор продолжил:
Еще один положительный инотропный агент, который следует учитывать, это милринон, поскольку он снижает ОПСС и увеличивает сердечный выброс; однако следует действовать с осторожностью, поскольку фармакологический механизм милринона может вызвать расширение сосудов и усугубить гипотензию.
Когда прессоры не могут поддерживать артериальное давление, можно рассмотреть возможность баллонной вальвулопластики. Это процедура была рекомендована в качестве моста к хирургическому вмешательству тем, кто не является кандидатом на операцию.5 К сожалению, ее доступность обычно ограничена крупными медицинскими центрами.6,7 Хирургическая коррекция АС посредством протезирования клапана является окончательным методом лечения такого заболевания. Тем не менее, следует отметить, что неотложное хирургическое вмешательство у пациентов с нестабильным АС связано со значительной смертностью, которая составляет от 30 до 50%.8
Вазодилатирующая терапия при критическом АС
Хотя нитропруссид неприменим в описанном выше случае, учитывая гипотензию пациента, он может быть подходящим для пациентов с отеком легких на фоне острой сердечной недостаточности, вторичной по отношению к АС. Хотя долгое время считалось, что он противопоказан при АС из-за преднагрузочно-зависимого состояния, были некоторые свидетельства того, что нитропруссид полезен для таких пациентов. В одном важном неконтролируемом исследовании нитропруссид, применяемый у пациентов с критическим АС и сердечной недостаточностью со сниженной фракцией выброса (средняя ФВ 21%, среднее СрАД 81 мм рт. ст.), показал значительное улучшение сердечного индекса без каких-либо эпизодов гипотонии, ишемических изменений ЭКГ, аритмии или одышки.9 Единственным критерием исключения из этого исследования была гипотензия, определяемая как потребность во внутривенном введении инотропных или прессорных агентов (добутамин, дофамин, адреналин, милринон, норадреналин или фенилэфрин), либо среднее системное артериальное давление ниже 60 мм рт. Среднее значение среднего системного АД для этих пациентов составило 81 +/- 13.
Кроме того, в исследовании сравнивали пациентов с АС и пациентов без АС при остром отеке легких, получавших нитраты. Не было существенной разницы между процентом пациентов в каждой группе, у которых развилась гипотензия после начала терапии. Однако было отмечено, что после того, как у этих пациентов действительно развилась гипотензия, у пациентов с умеренным и тяжелым АС с большей вероятностью сохранялась гипотензия, несмотря на вмешательства10.
Руководство ACC/AHA по ведению пациентов с клапанной болезнью сердца 2014 года (The 2014 ACC/AHA guidelines for the Management of Patients with Valvular Heart Disease), ссылающееся на эту статью, содержат следующие рекомендации:
«КЛАСС IIb 1. Вазодилатирующая терапия может быть разумной, если она используется с инвазивным гемодинамическим мониторингом при неотложном лечении пациентов с тяжелым декомпенсированным АС (стадия D) с симптомами сердечной недостаточности IV класса по NYHA (Уровень достоверности: C) У пациентов с тяжелой формой АС и классом ХСН IV по NYHA, снижение постнагрузки может использоваться для стабилизации состояния пациента перед неотложным протезированием клапанов. Инвазивный мониторинг давления наполнения ЛЖ, сердечного выброса и системного сосудистого сопротивления имеет важное значение из-за слабого гемодинамического статуса этих пациентов в у которых внезапное снижение системного сосудистого сопротивления может привести к резкому снижению сердечного выброса через обструкцию аортального клапана. Однако некоторым пациентам действительно помогает увеличение сердечного выброса, поскольку системное сосудистое сопротивление медленно снижается из-за снижения постнагрузки ЛЖ. У таких пациентов следует проводить хирургическую коррекцию порока как можно скорее».
ЗАКЛЮЧЕНИЕ
Переменные, которые взаимодействуют в случаях тяжелого стеноза аорты, являются причиной того, что таких пациентов так сложно лечить, а особые методы лечения, направленные на решение одной проблемы, часто ухудшают последствия другой проблемы. Если кто-то страдает респираторной недостаточностью, его дыхательные пути и дыхание необходимо защитить неинвазивными или инвазивными способами. Далее необходимо стабилизировать артериальное давление пациента. Часто наиболее подходящим агентом будет препарат с положительным инотропным действием, с учетом вазоактивного агента при стойкой гипотензии. После стабилизации состояния пациента можно определить степень повреждения миокарда и составить план окончательного лечения.
Комментарий Смита
При лечении кардиогенного шока поддерживающая терапия часто упускается из виду. Работа дыхания требует значительного сердечного выброса и, следовательно, нагружает сердце. Искусственная вентиляция легких с миорелаксацией устраняет до 50% потребности в кислороде и может дать отдых сердцу. Я бы сразу же интубировал такого тяжелого пациента.
Что касается других инвазивных методов лечения, внутриаортальная баллонная контрпульсация (12, 13), по-видимому, хорошо работает в нерандомизированных исследованиях, и это также имеет смысл: баллон в аорте раздувается в диастоле, увеличивая диастолическое давление и, следовательно, коронарный кровоток. Он также сдувается во время систолы, что обычно снижает постнагрузку; однако при стенозе аорты постнагрузка определяется главным образом клапаном, а не постклапанным сопротивлением.
Заключительный комментарий Смита
Неясно, что послужило причиной нестабильности этого пациента. Любое изменение физиологии может изменить «компенсированный» АС на «декомпенсированный». Например: сепсис, кровотечение, обезвоживание, гипоксия и легкая форма ОКС. У этого пациента была небольшая полость ЛЖ, что необычно для лиц с АС, плохой функцией ЛЖ и высоким давлением наполнения, но, вероятно, из-за тяжелой ГЛЖ. Поскольку давление наполнения ЛЖ оказалось высоким, эта небольшая полость ЛЖ не могла быть результатом истощения объема. В любом случае, когда АС становится декомпенсированным по какой-либо причине, с ним чрезвычайно трудно справиться из-за низкого давления коронарной перфузии и высокой потребности в кислороде.
ССЫЛКИ
- Taglieri N, Marzocchi A, Saia F, et al. Short- and long-term prognostic significance of ST-segment elevation in lead aVR in patients with non-ST-segment elevation acute coronary syndrome. Am J Cardiol 2011;108:21-8.
- Kosuge M, Ebina T, Hibi K, et al. An early and simple predictor of severe left main and/or three-vessel disease in patients with non-ST-segment elevation acute coronary syndrome. Am J Cardiol 2011;107:495-500.
- Overgaard, Christopher; Dzavik, Vladimir. Contemporary Reviews in Cardiovascular Medicine. Inotropes and Vasopressors: Review of Physiology and Clinical Use in Cardiovascular Medicine. Circulation. 2008;118:1047-1056.
- Richard, C; et al. Combined Hemodynamic Effects of Dopamine and Dobutamine in Cardiogenic Shock. Circulation 67, No. 3, 1983.
- Safian RD, Berman AD, Diver DJ, et al. Balloon aortic valvuloplasty in 170 consecutive patients. N Engl J Med 1988;319:125-30
- Rahimtoola SH. Catheter balloon valvuloplasty for severe calcific aortic stenosis: a limited role. J Am Coll Cardiol 1994;23:1076-1078
- Moreno PR, Jang IK, Newell JB, Block PC, Palacios IF. The role of percutaneous aortic balloon valvuloplasty in patients with cardiogenic shock and critical aortic stenosis. J Am Coll Cardiol 1994;23:1071-1075
- Hutter AM Jr, De Sanctis RW, Nathan MJ, et al. Aortic valve surgery as an emergency procedure. Circulation 1970;41:623-627
- Umesh N. Khot, MD; et al. Nitroprusside in Critically Ill Patients with Left Ventricular Dysfunction and Aortic Stenosis. N Engl J Med 2003; 348:1756-1763, 5/1/2013.
- Claveau, D; et al. Complications Associated with Nitrate Use in Patients Presenting with Acute Pulmonary Edema and Concomitant Moderate or Severe Aortic Stenosis. Annals of Emergency Medicine. 2015 Oct; 66(4):355-362.
- De Backer D et al. Comparison of Dopamine and Norepinephrine in the Treatment of Shock. NEJM 362(9):779; March 4, 2009.
- Folland ED, et al. Intraaortic Balloon Counterpulsation as a temporary support measure in decompensated critical aortic stenosis. J Am Coll Cardiol. 1985;5(3):711-716. http://content.onlinejacc.org/article.aspx?articleid=1111078
- Olcay A. et al. Cardiogenic shock in the setting of severe aortic stenosis: role of intra-aortic balloon pump support. Heart 2011;97:838-843 http://heart.bmj.com/content/97/10/838.short
- Nishimura RA and Otto CM, et al. 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease. Journal of the American College of Cardiology 63(22):e57-e185; June 10, 2014.