Можно ли локализовать виновное поражение на ангиограмме, не принимая во внимание изменения ЭКГ?
Автор: Вилли Фрик (Can you localize the culprit lesion on angiogram without taking ECG findings into account?)
Женщина примерно 60 лет с очень тяжелой гиперлипидемией (ЛПНП >6 ммоль/л) обратилась с острой болью в груди. Симптомы начались, когда она вышла из автобуса. Она описала боль как умеренную по интенсивности и сказала, что она появлялась и исчезала несколько раз в течение следующих нескольких часов, прежде чем окончательно исчезла. В день обращения боль вернулась и была очень сильной с сопутствующей одышкой и рвотой. Учитывая это, предтестовая вероятность ИМО очень высока. Достаточно высока, чтобы невыразительная ЭКГ не сразу успокаивала.
ЭКГ 1
Что вы думаете?
Для меня эта ЭКГ не является диагностической. Нижние зубцы T немного великоваты, но они могут быть такими исходно. В прекардиальной области низкий вольтаж, что всегда затрудняет диагностику ишемии. В сегменте ST в V2-3 наблюдается какая-то пугающая сглаженность. Но если вы назовете каждую ЭКГ, похожую на эту, ИМО, у вас будет много ложноположительных результатов. В отделении неотложной помощи пациентке дали нитроглицериновую пасту. Боль не прошла, поэтому ей дали таблетку нитроглицерина и внутривенно ввели морфин с разрешением боли.
Смит: это очень подозрительно для нижнего ИМО, но не на 100% диагностично. Имеются некоторые морфологические признаки ГЛЖ, но не амплитуды. Королева Червей не диагностирует ИМО.
При ОКС боль в груди является предупреждающим признаком продолжающейся ишемии. Я уже говорил, что лечение стенокардии морфином и продолжение неэкстренного лечения — это как вынуть батарейки из активно сработавшего детектора дыма во время пожара дома и снова лечь спать.
Смит: Как говорит Вилли, и как мы уже много раз говорили, морфин снимает боль, не устраняя ишемию. Поэтому следует предполагать продолжающиеся симптомы, если были даны опиаты. Давайте опиаты ТОЛЬКО в случае невыносимой боли, иначе вы активируете лабораторию катетеризации при первых объективных признаках коронарной ишемии.
Далее в течение оставшегося дня ЭКГ не регистрировались. Первый высокочувствительный тропонин I (hsTnI) составил 745 нг/л.
Смит: На данном этапе это острый инфаркт миокарда с предполагаемыми устойчивыми рефрактерными симптомами, и следует активировать экстренную катетеризацию.
Продолжение случая
Увы, это простое правило было проигнорировано.
Последующие тропонины поднялись: 588 нг/л и 4189 нг/л (URL: < 14 нг/л). Следующая запись взята из телеметрии около полуночи:
Из обзора стационарной карты следует, что ФЖ сохранялась в течение 20 минут до успешного прекращения. Документация показывает, что пациентке был нанесен разряд 4 раза (без комментариев по уровню энергии) и ей был введен амиодарон 300 мг внутривенно и магний 2 г внутривенно. Выведение пациентов из ЖТ/ФЖ является приоритетом номер один. Разряд может не сработать по двум причинам, и это можно решить двумя разными подходами:
- Разряд прекращает ЖТ/ФЖ, но затем она немедленно возвращается
- Разряд никогда не прекращает ЖТ/ФЖ, даже на секунду
В первом случае разряд выполнил свою задачу, но есть и другие факторы, способствующие ЖТ/ФЖ, такие как неваскуляризированная ишемия. В этом случае вы можете дать антиаритмические препараты и устранить основную причину (ИМО). Во втором случае ритм у пациента так и не восстановился, что означает, что разряд вообще не выполнил свою задачу. В этом случае вам следует взять второй дефибриллятор и выполнить двойную последовательную наружную дефибрилляцию (ДПНД). Просто подключите второй дефибриллятор, как показано на схеме ниже, и одновременно подавайте максимальные разряды с обоих устройств.
Смит: часто врачи думают, что указанный выше ритм — это торсада (или полиморфная ЖТ из-за удлиненного QT). Но торсада и фибрилляция желудочков не могут быть различены монитором. Их можно различить только по:
1) если есть пульс, то это не ФЖ
2) если она спонтанно разрешается, то это не ФЖ, за редкими исключениями
DOSE VF, New England Journal 2022 (ЕД - единственная дефибрилляция, ИВ - изменение вектора дефибрилляции)
Помните, что в исследовании DOSE VF догоспитальное использование ДПНД увеличило вероятность выживания до выписки из больницы на 17,1% в абсолютном выражении! Это число, необходимое для лечения чуть менее 6, и это почти ничего не стоит.
Возвращаемся к случаю:
Повторная ЭКГ после восстановления спонтанного кровообращения.
ЭКГ 2
Теперь у нас есть четкий нижний, задний и боковой ИМО. Пациентка была доставлена в рентгеноперационную для коронарной ангиографии. Для этого поста я включил самую важную ангиограмму с моим комментарием. Остальные ангиограммы здесь.
А вот мое комментированное объяснение:
У пациентки было проведено вмешательство на проксимальной ЛПНА. Вмешательство на ОА не проводилось. В отчете говорится, что была «окклюзия небольшой боковой ветви». Повторная ЭКГ через двенадцать часов показана ниже.
ЭКГ 3
Эта ЭКГ показывает постоянную заднебоковую окклюзию. Нижний инфаркт выглядит почти полным (выраженные зубцы Q с инверсией зубца T). Таким образом, похоже, что верхняя ЭКГ действительно была нижним ИМО. Нет никаких доказательств реперфузии, только прогрессия нелеченного инфаркта. Последовательные hsTnI, начавшиеся во время остановки сердца, составили 9652 нг/л, 12 747 нг/л и 21 112 нг/л. Дальнейшие проверки не проводились. Эхокардиограмма была технически сложной, но показала сохраненную фракцию выброса и средне-дистальный нижнебоковой гипокинез.
Пациентка оставалась интубированной в течение нескольких дней после этого. Даже после экстубации она не могла вспомнить события, приведшие к госпитализации, поэтому неизвестно, испытывала ли она постоянную боль в груди во время интубации после стентирования ЛНА. Она была в сознании и выполняла команды, но более конкретных подробностей о ее неврологическом обследовании нет.
Обсуждение:
Этот случай, скорее всего, представляет собой еще один случай ЧКВ не того сосуда. В блоге было много подобных случаев. Я поделился этим случаем с несколькими людьми, и никто не был полностью уверен, какой сосуд был виновником.
Я думаю, что это, скорее всего, артерия тупого края по причинам, которые я упомянул в озвученном видео, однако стоит задаться вопросом, может ли такой маленький сосуд вызывать столь обширные изменения ЭКГ. И определенно возможно, что более проксимальное поражение ошибающей разорвалось и вызвало дистальную эмболию. Некоторые другие беспокоились о ПКА как о возможном виновнике.
Неопределенность относительно виновного сосуда очень распространена. Фактически, в этом элегантном исследовании Хайтнера и соавторов исследователи обнаружили, что среди пациентов, получивших реваскуляризацию, 27% получили реваскуляризацию исключительно невиновных коронарных артерий!
Исследование 2017 года под названием CULPRIT SHOCK показало, что у пациентов с кардиогенным шоком стратегия ЧКВ только виновного сосуда была связана с лучшими результатами, чем немедленное многососудистое ЧКВ. После CULPRIT SHOCK многие избегали многососудистого ЧКВ в острых ситуациях. Однако мы должны учитывать две вещи при переносе этих доказательств в клиническую практику. Во-первых, это были пациенты в шоке. И, во-вторых, это предполагает четкое определение виновника (критерий включения в это исследование). У многих пациентов может не быть четкого виновника.
Другие исследования обнаружили пользу реваскуляризации невиновных поражений, когда у пациента ОКС, самым крупным из которых был COMPLETE, а совсем недавно и MULTISTARS AMI. Хотя я верю результатам этих испытаний, у меня всегда были проблемы с сопоставлением этих результатов с результатами COURAGE, BARI 2D, ISCHEMIA, REVIVED-BCIS2, которые показали, что стентирование стабильных поражений не приводит к улучшению основных неблагоприятных сердечно-сосудистых событий (MACE). А в исследовании, таком как COMPLETE или MULTISTARS AMI, вы стентируете острый разрыв бляшки (виновник) и неразорвавшиеся, невиновные и, следовательно, по сути стабильные бляшки.
Итак, подведем итог. У нас есть доказательства того, что:
- Очень распространено ЧКВ неправильного сосуда, возможно, почти у трети пациентов (Heitner et al.)
- Стентирование стабильных поражений у большинства пациентов не снижает MACE (COURAGE, BARI 2D, ISCHEMIA, REVIVED-BCIS2)
- Стентирование всех поражений (стабильных и нестабильных) у пациентов с ОКС снижает MACE (COMPLETE, MULTISTARS AMI)
Возникает вопрос, может ли польза, наблюдаемая при COMPLETE и MULTISTARS AMI, быть частично обусловлена снижением или устранением возможности пропуска виновника?
Тем более, что для выявления разрыва бляшки и подтверждения виновника следует использовать внутрисосудистую визуализацию (ВСУЗИ или ОКТ), особенно с учетом того, что использование внутрисосудистой визуализации снижает смертность от всех причин на 25%.
Комментарий КЕНА ГРЭУЭРА, доктора медицины:
Я бы предложил в качестве одной из «тем» для сегодняшнего наводящего на размышления случая доктора Фрика — «Назад к основам» — несоблюдение этой фундаментальной концепции привело к печальным событиям в сегодняшнем случае.
- У пациента с высоким риском (как и сегодняшняя пациентка) — Если начальная ЭКГ перегружена артефактами, которые мешают точной интерпретации — то немедленно повторите ЭКГ. Вместо этого — ЭКГ не повторялась в течение оставшейся части дня.
- Даже если бы артефактов вообще не было — у пациента с высоким риском и продолжающимися симптомами ЭКГ следует повторять каждые 15–30 минут, пока не будет поставлен окончательный диагноз.
- Как описано выше доктором Фриком: был введен морфин — тропонины были повышены и росли — однако катетеризация сердца была отложена (ее провели только после длительной реанимации, которой, возможно, можно было бы избежать, если бы соблюдались основы).
- И, возможно, потому что при катетеризации было обнаружено многососудистое заболевание без явного «виновника» — ЧКВ было применено к неправильной артерии. По словам доктора Фрика — использование внутрисосудистой визуализации (ВСУЗИ или ОКТ) могло бы помочь обнаружить разрыв бляшки и определить «истинного» виновника.
- Повторная частая регистрация серийных ЭКГ у этой пациентки также могло бы помочь выявить «сигнальные» изменения ST-T, которые бы выявили сосудистую область(и), способствующую острому событию.
Начальная ЭКГ:
Учитывая, насколько сильно это зависит от оценки начальной ЭКГ, эту начальную ЭКГ следует немедленно повторить, если ее невозможно адекватно интерпретировать.
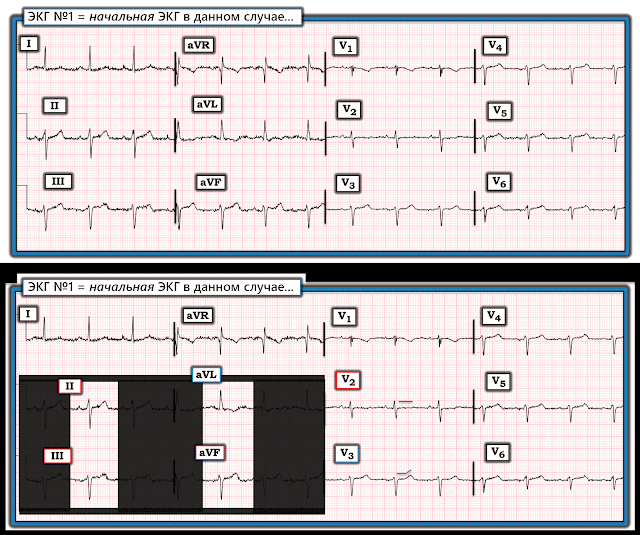
- Чтобы проиллюстрировать этот момент на рисунке 1, я воспроизвел сегодняшнюю начальную запись на ВЕРХНЕЙ панели. Артефакт изолинии явно искажает морфологию ST-T в каждом из 6 отведений от конечностей.
- ВОПРОС: Какой из 3 или 4 комплексов QRST в отведениях II, III, aVF — и в отведении aVL — демонстрируется «истинная» морфология ST-T в этих отведениях?
На НИЖНЕЙ панели рисунка 1 я выбрал средний комплекс QRST.
- У сегодняшней женщины 60+ лет с впервые выявленной тяжелой болью в груди — ЕСЛИ ST-T, которые я показываю на НИЖНЕЙ панели, являются «истинным» представлением морфологии ST-T в этих 4 отведениях — Разве это не тревожно?
- По крайней мере, в отведениях II и aVF — я думал, что зубцы T выглядят непропорционально большими, чем ожидалось (возможно, острейшими) — с тем, что кажется реципрокной депрессией ST в отведении aVL.
- В этом контексте впервые выявленного тяжелой боли в груди и потенциального нижнего ИМО — я думал, что явно аномальное уплощение сегмента ST в отведении V2 и более тонкое (но тем не менее аномальное) распрямление сегмента ST в отведении V3 подтверждают мои опасения по поводу нижне-заднего ИМО.
Как мы узнаем, выбрал ли я «истинную» морфологию волны ST-T?
- Ответ: Мы не знаем — потому что «мусор вошел = мусор вышел» — и просто слишком много артефактов, чтобы что-то сказать. Возможно, если бы эта начальная ЭКГ была немедленно повторена — и за ней последовала вторая ЭКГ в течение 15–20 минут — мы могли бы увидеть достаточно «динамичных» изменений ST-T, чтобы квалифицировать это как острое событие, требующее немедленной катетеризации (и эпизод фибрилляции желудочков мог бы никогда не произойти).
Рисунок 1: Я разметил начальную ЭКГ в сегодняшнем случае.






Комментариев нет:
Отправить комментарий