Боль в груди разрешилась. Нужна ли неотложная катетеризация (здесь есть споры) и многое-многое другое.
Мужчина 50 лет с гипертонией и стажем курения от 20 до 40 лет поступил с жалобами на перемежающуюся боль в груди в течение последней недели, боль усиливалась при физической нагрузке, нескоро проходила после отдыха и никогда не возникает в состоянии покоя. Боль сопровождалась легкой одышкой при физической нагрузке. Иногда боль иррадировала в шею слева. Боль сохранялась по прибытии в клинику, но затем прошла еще до размещения в отделение неотложной помощи.
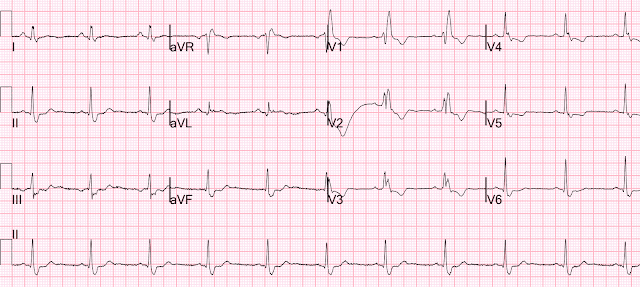
ЭКГ при поступлении:
Вот его предыдущая ЭКГ:
Нормальная элевация ST
Интерпретация ординатора: картина реперфузии/Wellens с двухфазными зубцами Т в V2 и V3, и по сравнению с ЭКГ 2020 года это новое нарушение.
Назначения: аспирин 325 мг, биохимический анализ крови, анализ тропонина (все взято). Прикроватное УЗИ без видимых нарушений движения стенок, без выпота в перикарде, без перегрузки правого сердца, аорта при кратком осмотре выглядит нормального диаметра с нормальными стенками.
Повторная ЭКГ:
Интерпретация ординатора: элевация ST в V2 существенно больше, чем на предыдущей ЭКГ. У пациента по-прежнему нет боли в груди, однако это все больше похоже на ИМО/ИМпST. Его перевели в палату наблюдения перед катетеризацией. Лабораторные показатели еще не готовы. Дан аспирин.
Смит: Я не думаю, что действительно есть какие-либо изменения в элевации ST. Эти изменения связаны с изменением расположения электродов: на первой ЭКГ (вверху) отведения V1 и V2 были расположены слишком высоко (инвертированный зубец P). Это приводит к регистрации меньшей элевации ST в отведении V2. На более поздней, 2-й ЭКГ, отведения расположены правильно, и элевация ST кажется большей.
Это стабильная ЭКГ. Пациент без боли и у него явно имеется синдром Велленса: 1) отсутствие боли после приступа стенокардии, типичный паттерн А (двухфазный, терминальная инверсия зубца Т с начальным восходящим сегментом ST), сохраненный зубец R. Паттерн B приводит к глубокой симметричнуой инверсии зубца Т без начальной восходящей элевации ST. Паттерн А развивается в Паттерн B.
Это отличная серия ЭКГ, демонстрирующая эволюцию: Доктор Смит показывает: Классическая эволюция зубцов Т Wellens в течение 26 часов
Требует ли синдром Велленса экстренной катетеризации? Или антиагрегантная и антитромботическая терапия адекватна для предотвращения повторной окклюзии перед отсроченным вмешательством?
Синдром Велленса — это синдром транзиторного ИМО (старая терминология — транзиторный ИМпST).
Вот прекрасная демонстрация того, что Wellens это транзиторный ИМО: Первая ЭКГ в отделении неотложной помощи - Wellens' (без боли). Как вы думаете, как выглядела догоспитальная ЭКГ (на фоне боли)?
А это статьи самого Велленса, показывающая, как возникают волны Welelns после реперфузии тромболитиками (соавторы - Wehrens and Doevendans соответственно).
- Wehrens XH, Doevendans PA, Ophuis TJ, Wellens HJ. A comparison of electrocardiographic changes during reperfusion of acute myocardial infarction by thrombolysis or percutaneous transluminal coronary angioplasty. Am Heart J. 2000;139:430–436.
- Doevendans PA, Gorgels AP, van der Zee R, Partouns J, Bar FW, Wellens HJJ. Electrocardiographic diagnosis of reperfusion during thrombolytic therapy in acute myocardial infarction. Am J Cardiol. 1995;75:1206–1210.
Насколько я могу судить, существует только одно рандомизированное исследование немедленного и отсроченного вмешательства при транзиторном ИМпST. (Не существует рандомизированных или даже обсервационных исследований немедленного или отсроченного вмешательства при синдроме Велленса.)
Lemkes JS, et al. Timing of revascularization in patients with transient ST-segment elevation myocardial infarction: a randomized clinical trial. Eur Heart J [Internet]. 2019;40:283–291. Available from: http://dx.doi.org/10.1093/eurheartj/ehy651.
В этом исследовании основные исходы были одинаковыми для обеих групп, но из 70 пациентов в группе с отсроченной окклюзией 4 потребовали экстренного вмешательства из-за внезапной повторной окклюзии. Выводы можете сделать самостоятельно.
Думаю, мне хотелось бы вмешаться до того, как возникнет риск повторной окклюзии.
Тем не менее, можно привести разумный аргумент в пользу отсрочки, особенно если вам придется разбудить вашу команду интервенционистов посреди ночи. При синдроме Wellens требуется полная антиагрегантная и антитромботическая терапия, и, по моему мнению, если вы откладываете лечение, вам следует постоянно мониторировать ЭКГ в 12 отведениях.
Вот почему:
1. Почему при синдроме Wellens необходим непрерывный мониторинг сегмента ST в 12 отведениях
2. Синдром Wellens, виновника нет, что случилось?
____________________
Продолжение
Экстренная катетеризации была активирована через 70 минут после прибытия в отделение неотложной помощи./p>
Первый hs тропонин I через 108 минут после прибытия в отделение неотложной помощи был в норме: 12 нг/л.
___________________
В отделении неотложной помощи P2Y12 до ангиографии» не назначался (т.е. до того, как ангиограмма определит анатомию коронарных артерий). Часто назначают P2Y12 еще до ангиграфии, но, судя по литературе, польза ограничена, особенно потому, что кангрелор можно вводить внутривенно во время ангиографии, после того как определена анатомия коронарных артерий. Таким образом, если есть необходимость в АКШ, операцию не нужно откладывать из-за риска кровотечения из-за стойкого ингибирования P2Y12.
Документ по P2Y12: https://www.nejm.org/doi/full/10.1056/nejmoa1407024
Таким образом, в данном случае тикагрелор не назначался.
Ангиография:
- Виновником нестабильной стенокардии/синдрома Веллена у пациента является разрыв бляшки в средней части ПМЖВ.
- В соответствии с ЭКГ, на начальной ангиографии имеется поток TIMI-3.
- ПМЖВ - сосуд крупного калибра, доходящий до верхушки.
- При начальной ангиографии имеется стеноз средней части ПМЖВ от 80 до 90% с вкровотоком TIMI-3.
- Это поражение имеет ангиографические характеристики разрыва бляшки и, вероятно, является причиной синдрома Велленса/нестабильной стенокардии у пациента.
Кангрелор назначен после определения коронарной анатомии
Повреждение было стентировано
Пиковый уровень тропонина составил 108 нг/л. Полная коронарная окклюзия, если она очень кратковременная, может привести к минимальному инфаркту, но при этом быть очень опасной.
Эхо:
- Нормальный размер полости левого желудочка и нормальная систолическая функция ЛЖ.
- Нормальная расчетная фракция выброса левого желудочка 54%.
- Региональные нарушения движения стенок – апикальная перегородка и верхушка, гипокинез.
- Увеличение толщины стенки ЛЖ, асимметричное (см. ниже).
- Нормальный размер и функция правого желудочка.
Таким образом, даже при этом очень небольшом инфаркте наблюдалось оглушение миокарда (нарушение движения стенки при отсутствии значительного инфаркта). Это обычное явление, и стенка почти всегда восстанавливается примерно в течение 6 недель.
Вот еще очень интересные публикации:
Вот множество примеров очень распространенной имитации, которую мы называем «доброкачественной инверсией зубца Т» и которая является вариантом ранней реполяции: Понимание этой патогномоничной ЭКГ принесло бы большую пользу пациенту
Комментарий Кена Грауэра, доктора медицины:
Когда мы говорим о синдроме Велленса, все зависит от времени. Несмотря на описание синдрома Велленса более 40 лет назад, этот синдром по-прежнему неправильно понимается большинством клиницистов (см. комментарий в сообщении Нижняя элевация ST и острейшие зубцы T, но у пациента боли нет. Что происходит?).
Первоначальными исследователями в 1982 году были описаны два паттерна ЭКГ как соответствующие развитию синдрома Велленса при стенозе ПМЖВ высокой степени.
- Паттерн B — более распространенная форма в оригинальном отчете Велленса. По моему опыту, этот паттерн ЭКГ менее специфичен для стеноза ПМЖВ высокой степени, поскольку другие состояния (включая несердечные заболевания ЦНС) также могут быть связаны с симметричной инверсией зубца Т.
- Напротив, Паттерн А по оригинальному отчету Велленса был гораздо менее распространен. Тем не менее, когда анамнез «подходящий» для синдрома Велленса, крутой спуск зубца Т от пика зубца Т, характерный для Паттерна А, по моему мнению, более специфичен, чем симметричная инверсия зубца Т при Паттерне B.
- На исходной ЭКГ из сегодняшнего случая картина ST-T в светло-синих прямоугольниках на рисунке 1 соответствует более специфическому ЭКГ паттерну A. Это особенно верно для ST-T в отведении V3, в котором снижение зубца Т от пика вогнутого и слегка приподнятого сегмента ST чрезвычайно крутой (= еще один пример состояния ЭКГ, при котором картина «стоит 1000 слов» — потому что форма этого крутого спуска зубца Т уникальна).
Непонятые особенности Wellens:
- Для наличия синдрома Велленса в анамнезе должно быть указание на предшествующую боль в груди, которая уже прошла на момент записи ЭКГ. Если боль в груди все еще присутствует, то это не синдром Велленса. Вместо этого может наблюдаться стойкая боль в груди, указывающая на продолжающийся инфаркт и/или реперфузионные зубцы Т, которые развиваются после завершенного события.
- Именно патофизиологию истинного «синдрома Велленса» обычно неправильно понимают, поскольку имеет место временная коронарная окклюзия, которая затем спонтанно разрешается, что приводит к разрешению боли в груди (и не более чем к минимальному повреждению миокарда).
- Вышеуказанная патофизиология является причиной того, что признание д-ром Смитом того, что на повторной ЭКГ в сегодняшнем случае нет динамических изменений, важно. Это связано с тем, что по приведенному выше обоснованию распознавание синдрома Велленса подразумевает временно «стабильную» ситуацию после того, как произошла спонтанная реперфузия «виновного» поражения ПМЖВ.
- Согласно приведенному выше обзору современной литературы по этому вопросу, проведенному д-ром Смитом, может показаться, что немедленная катетеризация при ЧКВ у пациента с синдромом Велленса предпочтительнее тщательного наблюдения, пока вы ждете и надеетесь, что вам не придется делать экстренную катетеризацию, ЕСЛИ «сосуд-виновник» повторно закупоривается. И, учитывая, что такая повторная окклюзия «сосуда-виновника» может произойти практически в любое время после спонтанной реперфузии (т.е. через несколько часов или даже дней) — Что, ЕСЛИ спонтанная реокклюзия произойдет после того, как пациента отправили домой, потому что «ничего не произошло» в течение 1-2 дней, пока пациент находился под наблюдением в больнице?
Рисунок 1: В сегодняшнем случае я разметил исходную ЭКГ.
Дополнительные выводы:
Я думал, что КЛЮЧЕВОЙ клинический момент, подчеркнутый проницательным рассказом доктора Смита о сегодняшнем случае, заключается в том, насколько быстро можно поставить диагноз синдрома Велленса.
- Очевидно, что сравнение ЭКГ № 1 с предыдущей ЭКГ сегодняшнего пациента подтвердило, что крутой наклон зубца Т в сочетании с передней инверсией зубца Т был новым открытием, НО — предыдущие записи не всегда доступны — и даже ЕСЛИ эта предыдущая ЭКГ не была бы найдена — диагноз синдрома Велленса уже был подтвержден кратким анамнезом, согласно которому у пациента разрешилась боль в груди в тот момент, когда на исходной ЭКГ был виден уникальный крутой нисходящий передний зубец Т.
- Отрезвляющее замечание: необходимость срочной катетеризации в сегодняшнем случае была оценена только после того, как была сделана вторая ЭКГ, в ходе которой изменение расположения отведений привело к ошибочному заключению, что имеется нарастание элевации ST (см. мой комментарий в сообщении Что это за элевация ST?, посвященная обзору того, как распознать слишком высокое расположение электродов V1, V2).
Последние мысли:
- Диагностика синдрома Велленса в сегодняшнем случае была затруднена, поскольку у этого мужчины 50 лет с гипертонией на ЭКГ имеется ГЛЖ (по критериям Пегуеро — как сумма S 25 мм в V3 + S 13 мм в V4 >28 мм — в соответствии с критериями ГЛЖ, которые я подробно описал на рисунке 3 в вышеуказанной публикации).
- Тем не менее, «перегрузка» ЛЖ никогда не должна выглядеть как крутой спуск зубца Т, который мы видим в отведении V3 на рисунке 1, на котором нет признаков «перегрузки» ЛЖ в боковых грудных отведениях.
- ИТОГ: История сегодняшнего случая новой боли в груди, которая разрешилась к тому времени, когда была сделана первоначальная ЭКГ, показывающая уникальный крутой нисходящий зубец Т с его инверсией в передних отведениях, должна позволить немедленно распознать синдром Велленса. Судя по тому, что мы знаем о патофизиологии синдрома Велленса, кажется, что чем раньше можно будет организовать катетеризацию с помощью ЧКВ, тем больше шансов на оптимальный результат.